Ingin mempelajari materi kimia, khususnya tentang Gaya Dispersi London? Supaya lebih paham, kamu bisa menyimak pembelajarannya di sini. Kamu juga bisa mengerjakan soal latihan untuk mempraktikkan materi yang telah dijelaskan.
Lewat pembahasan ini, kamu bisa belajar mengenai Gaya Dispersi London. kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Kamu juga akan memperoleh latihan soal interaktif yang tersedia dalam tiga tingkat kesulitan, yaitu mudah, sedang, dan sukar. Tertarik untuk mempelajarinya?
Sekarang, kamu bisa mulai mempelajari materi lewat uraian berikut. Apabila materi ini berguna, bagikan ke teman-teman kamu supaya mereka juga mendapatkan manfaatnya.
Kamu dapat download modul & contoh soal serta kumpulan latihan soal Gaya Dispersi London dalam bentuk pdf pada link dibawah ini:
Definisi
Gaya tarik antar molekul yang diakibatkan terbentuknya kutub muatan (dipol) sementara/ sesaat.
Gaya Dispersi London
Teori mengenai gaya dispersi/ gaya London dikembangkan untuk menjelaskan interaksi intermolekul pada senyawa non-polar. Awalnya sesuai teori yang ada, jika sesama molekul non-polar saling mendekati maka akan terjadi gaya tolak-menolak diantara awan elektron pada permukaannya.
Akan tetapi, fakta menunjukkan bahwa suatu molekul non-polar dapat dicairkan, dimana ini hanya dimungkinkan bila terdapat suatu gaya antarmolekul yang menyatukan molekul-molekul dalam wujud cair.
Pada 1928, seorang ilmuwan Jerman, Fritz London, dapat mengemukakan suatu penjelasan teoritis yang masuk akal tentang gaya antarmolekul dalam zat yang non-polar, oleh sebab itu gaya ini disebut juga gaya London. Penjelasannya adalah sebagai berikut.
Elektron yang selalu bergerak dalam orbital menyebabkan pada suatu waktu yang singkat terjadi distribusi elektron yang tidak merata, sehingga terbentuk kutub muatan atau dipol sesaat.
Dipol sesaat ini kemudian akan menginduksi terbentuknya dipol sesaat pada molekul lainnya, sehingga hasilnya adalah suatu gaya tarik-menarik antarmolekul yang lemah, seperti digambarkan pada diagram berikut:
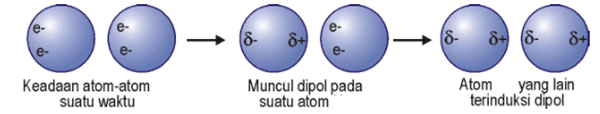
Kekuatan gaya dispersi suatu molekul tergantung kepada:
1. Luas permukaannya.
Semakin besar luas permukaan maka semakin kuat gaya dispersinya yang terlihat dari titik didih yang semakin tinggi. Contohnya titik didih Neon (Ne) lebih kecil daripada metana $\mbox{CH}_{4}$, karena Luas permukaan metana lebih besar daripada neon, atau dapat kita jumpai pada senyawa organik.
Misalnya untuk alkana rantai lurus mempunyai titik didih lebih tinggi daripada senyawa alkana rantai bercabang dengan rumus molekul yang sama.
2. Jumlah elektron / Mr senyawa.
Sebenarnya Mr ini berkaitan dengan jumlah elektron. Di mana jumlah elektron sebanding Mr nya.
Contohnya, $\mbox{Cl}_{2}$ mempunyai titik didih lebih kecil daripada $\mbox{Br}_{2}$ . Karena jumlah elektron Br lebih banyak (Mr lebih besar pula) sehingga gaya van der Waals nya lebih kuat.
Contoh Soal Gaya Dispersi London dan Pembahasan
Tentukan manakah diantara molekul berikut yang akan memiliki titik didih lebih tinggi?
- gas nitrogen dan gas oksigen
- butana dan isobutana
Jawaban
- $\mbox{N}_{2}$, memiliki Mr = 28. $\mbox{O}_{2}$ memiliki Mr = 32. Sehingga gas oksigen akan memiliki titik didih lebih tinggi karena mempunyai gaya van der Waals yang lebih kuat.
- Butana memiliki susunan rantai lurus sementara isobutana memiliki susunan rantai bercabang. Sehingga butana akan memiliki luas permukaan yang lebih besar, dengan titik didih yang lebih tinggi dari isobutana.
Latihan Soal Gaya Dispersi London (Mudah)
Ringkasan kuis
0 dari 5 pertanyaan telah diselesaikan
Pertanyaan:
- 1
- 2
- 3
- 4
- 5
Informasi
You have already completed the quiz before. Hence you can not start it again.
Quiz is loading...
Anda harus masuk atau mendaftar untuk memulai kuis.
Anda harus menyelesaikan kuis dibawah ini, untuk memulai kuis ini:
Hasil
Hasil
0 dari 5 pertanyaan terjawab dengan benar
Waktu yang telah berlalu
Kategori
- Tidak Berkategori 0%
- 1
- 2
- 3
- 4
- 5
- Terjawab
- Tinjau
-
Pertanyaan ke 1 dari 5
1. Pertanyaan
Interaksi intermolekuler meliputi …
BetulInteraksi intermolekuler meliputi ikatan hidrogen, interaksi dipol dan gaya London.
SalahInteraksi intermolekuler meliputi ikatan hidrogen, interaksi dipol dan gaya London.
-
Pertanyaan ke 2 dari 5
2. Pertanyaan
Berikut ini interaksi intermolekuler yang dapat dimiliki semua molekul adalah …
BetulInteraksi intermolekuler yang terjadi pada semua jenis molekul hanyalah gaya London.
SalahInteraksi intermolekuler yang terjadi pada semua jenis molekul hanyalah gaya London.
-
Pertanyaan ke 3 dari 5
3. Pertanyaan
Suatu zat atau senyawa pada fase … memiliki interaksi intermolekuler paling besar …
BetulPada fase padat jarak antar molekul sangat berdekatan sehingga pada fase inilah terjadinya interaksi intermolekuler yang paling kuat.
SalahPada fase padat jarak antar molekul sangat berdekatan sehingga pada fase inilah terjadinya interaksi intermolekuler yang paling kuat.
-
Pertanyaan ke 4 dari 5
4. Pertanyaan
Interaksi intermolekular yang terjadi pada semua molekul disebabkan karena terbentuknya …
BetulGaya London terjadi akibat terbentuknya momen dipol tak permanen pada molekul tersebut.
SalahGaya London terjadi akibat terbentuknya momen dipol tak permanen pada molekul tersebut.
-
Pertanyaan ke 5 dari 5
5. Pertanyaan
Interaksi intermolekuler berikut yang mempengaruhi besarnya titik didih suatu senyawa adalah …
BetulSemua interaksi intermolekuler mempengaruhi besarnya titik didih suatu senyawa.
SalahSemua interaksi intermolekuler mempengaruhi besarnya titik didih suatu senyawa.
Latihan Soal Gaya Dispersi London (Sedang)
Ringkasan kuis
0 dari 5 pertanyaan telah diselesaikan
Pertanyaan:
- 1
- 2
- 3
- 4
- 5
Informasi
You have already completed the quiz before. Hence you can not start it again.
Quiz is loading...
Anda harus masuk atau mendaftar untuk memulai kuis.
Anda harus menyelesaikan kuis dibawah ini, untuk memulai kuis ini:
Hasil
Hasil
0 dari 5 pertanyaan terjawab dengan benar
Waktu yang telah berlalu
Kategori
- Tidak Berkategori 0%
- 1
- 2
- 3
- 4
- 5
- Terjawab
- Tinjau
-
Pertanyaan ke 1 dari 5
1. Pertanyaan
Pada fase manakah interaksi intermolekuler di antara senyawa paling lemah?
BetulPada fase gas molekul memiliki jarak yang sangat berjauhan satu sama lain sehingga interaksi intermolekulernya paling lemah dibanding fase lainnya.
SalahPada fase gas molekul memiliki jarak yang sangat berjauhan satu sama lain sehingga interaksi intermolekulernya paling lemah dibanding fase lainnya.
-
Pertanyaan ke 2 dari 5
2. Pertanyaan
Berikut ini faktor yang mempengaruhi kuatnya gaya London adalah …
BetulFaktor yang mempengaruhi kuatnya gaya London antara lain adalah luas permukaan molekul.
SalahFaktor yang mempengaruhi kuatnya gaya London antara lain adalah luas permukaan molekul.
-
Pertanyaan ke 3 dari 5
3. Pertanyaan
Berikut ini adalah sifat dari gaya London, kecuali …
BetulGaya London tidak dipengaruhi oleh temperatur sistem.
SalahGaya London tidak dipengaruhi oleh temperatur sistem.
-
Pertanyaan ke 4 dari 5
4. Pertanyaan
Berikut ini senyawa yang tidak mempunyai ikatan permanen dipol-dipol adalah …
BetulSenyawa yang tidak mempunyai ikatan permanen dipol-dipol adalah senyawa non polar. Pilihan D merupakan senyawa non polar.
SalahSenyawa yang tidak mempunyai ikatan permanen dipol-dipol adalah senyawa non polar. Pilihan D merupakan senyawa non polar.
-
Pertanyaan ke 5 dari 5
5. Pertanyaan
Ikatan antar molekul berikut ini yang mempunyai ikatan antar molekul lebih kuat daripada $\mbox{CH}_{4}$ adalah … kecuali.
Betul$\mbox{CH}_{4}$ merupakan molekul non polar, ikatan antar molekul $\mbox{CH}_{4}$ adalah gaya London.
- $\mbox{HC}\ell$: ikatan dipol-dipol
- $\mbox{NH}_{3}$ : ikatan hidrogen
- $\mbox{O}_{2}$: gaya London
- $\mbox{CH}_{3}\mbox{CH}_{3}$: gaya London
- $\mbox{CH}_{3}\mbox{Br}$ : ikatan dipol-dipol
Kekuatan ikatan London tergantung pada ukuran molekulnya, ukuran partikel $\mbox{CH}_{3}\mbox{CH}$$>\mbox{CH}_{4}$$>\mbox{O}_{2}$ , semakin besar ukuran partikel semakin kuat London nya.
Salah$\mbox{CH}_{4}$ merupakan molekul non polar, ikatan antar molekul $\mbox{CH}_{4}$ adalah gaya London.
- $\mbox{HC}\ell$: ikatan dipol-dipol
- $\mbox{NH}_{3}$ : ikatan hidrogen
- $\mbox{O}_{2}$: gaya London
- $\mbox{CH}_{3}\mbox{CH}_{3}$: gaya London
- $\mbox{CH}_{3}\mbox{Br}$ : ikatan dipol-dipol
Kekuatan ikatan London tergantung pada ukuran molekulnya, ukuran partikel $\mbox{CH}_{3}\mbox{CH}$$>\mbox{CH}_{4}$$>\mbox{O}_{2}$ , semakin besar ukuran partikel semakin kuat London nya.
Latihan Soal Gaya Dispersi London (Sukar)
Ringkasan kuis
0 dari 5 pertanyaan telah diselesaikan
Pertanyaan:
- 1
- 2
- 3
- 4
- 5
Informasi
You have already completed the quiz before. Hence you can not start it again.
Quiz is loading...
Anda harus masuk atau mendaftar untuk memulai kuis.
Anda harus menyelesaikan kuis dibawah ini, untuk memulai kuis ini:
Hasil
Hasil
0 dari 5 pertanyaan terjawab dengan benar
Waktu yang telah berlalu
Kategori
- Tidak Berkategori 0%
- 1
- 2
- 3
- 4
- 5
- Terjawab
- Tinjau
-
Pertanyaan ke 1 dari 5
1. Pertanyaan
Gaya London dapat dilihat pada fenomena …
BetulGaya London berperan pada kemampuan tokek merayap di kaca, dimana interaksi terjadi antara permukaan kaca dengan rambut halus yang terdapat pada telapak kaki si tokek.
SalahGaya London berperan pada kemampuan tokek merayap di kaca, dimana interaksi terjadi antara permukaan kaca dengan rambut halus yang terdapat pada telapak kaki si tokek.
-
Pertanyaan ke 2 dari 5
2. Pertanyaan
Senyawa berikut ini yang paling volatil adalah …
BetulPaling volatil (mudah menguap) artinya mempunyai ikatan antar molekul yang paling lemah.
Urutan kekuatan gaya antar molekul adalah ikatan hidrogen $>$ ikatan dipol-dipol $>$ gaya London.SalahPaling volatil (mudah menguap) artinya mempunyai ikatan antar molekul yang paling lemah.
Urutan kekuatan gaya antar molekul adalah ikatan hidrogen $>$ ikatan dipol-dipol $>$ gaya London. -
Pertanyaan ke 3 dari 5
3. Pertanyaan
Diantara pernyataan berikut yang tepat adalah …
BetulPada teori gas ideal, semua interaksi intermolekuler diantara molekul gas diabaikan, termasuk gaya London.
SalahPada teori gas ideal, semua interaksi intermolekuler diantara molekul gas diabaikan, termasuk gaya London.
-
Pertanyaan ke 4 dari 5
4. Pertanyaan
Manakah diantara senyawa berikut ini yang akan memiliki titik didih paling tinggi?
BetulSemakin panjang rantai karbon maka semakin luas permukaan molekul, semakin besar gaya London nya dan semakin tinggi titik didihnya. Sementara semakin rapat suatu molekul, atau dalam kasus senyawa karbon, semakin banyak rantai cabangnya maka semakin menurun gaya London. Maka pentana, dengan rantai paling panjang dan tidak bercabang, akan memiliki titik didih paling tinggi.
SalahSemakin panjang rantai karbon maka semakin luas permukaan molekul, semakin besar gaya London nya dan semakin tinggi titik didihnya. Sementara semakin rapat suatu molekul, atau dalam kasus senyawa karbon, semakin banyak rantai cabangnya maka semakin menurun gaya London. Maka pentana, dengan rantai paling panjang dan tidak bercabang, akan memiliki titik didih paling tinggi.
-
Pertanyaan ke 5 dari 5
5. Pertanyaan
Diketahui beberapa senyawa dengan sifat sebagai berikut:

Manakah yang paling mungkin merupakan senyawa D?
BetulSemakin tinggi titik didih dan entalpi penguapan, semakin besar gaya London. Ingat dalam 1 golongan dari atas ke bawah ukuran unsur semakin besar, maka HI lah yang akan memiliki ukuran paling besar, dan gaya London yang paling besar pula.
SalahSemakin tinggi titik didih dan entalpi penguapan, semakin besar gaya London. Ingat dalam 1 golongan dari atas ke bawah ukuran unsur semakin besar, maka HI lah yang akan memiliki ukuran paling besar, dan gaya London yang paling besar pula.

